
Cálculo de valores para soluciones de electrolitos
¿Qué es una solución de electrolitos?
¿Has probado el agua de mar? Sabe terrible, ¿no? Esto se debe a que el agua en el océano no se compone solo de agua, sino que tiene sal mezclada. El agua salada del océano es en realidad un tipo de solución de electrolitos.
En general, una solución de electrolitos está hecha de cualquier sustancia que se disuelva en agua para formar una solución que conduzca la electricidad. Cuando el cloruro de sodio (una sal) se disuelve en agua, obtenemos una solución de agua de mar, ¡una solución de electrolitos!
Hoy, Rhonda está en el laboratorio de química tratando de poner algunos números a las soluciones de electrolitos que está manejando, pero ¿cómo puede hacerlo? Veamos cómo calcular las concentraciones de soluciones de electrolitos en función de tres unidades comunes de concentración: molaridad, molalidad y porcentaje en masa.
Nota: estas no son las únicas unidades de concentración disponibles para realizar este tipo de cálculo, pero son las unidades más comunes.
Revisión de término
Antes de pasar a los cálculos, repasemos algunos términos. Las soluciones se componen de dos cosas muy importantes:
- un soluto : el componente menor de la solución (es decir, lo que tiene menos)
- un solvente : el componente principal de la solución (es decir, lo que tiene más)
Al formar una solución, las partículas de disolvente rodean las partículas de soluto. Por ejemplo, si una solución contiene 10.0 gramos de cloruro de sodio en 100.0 gramos de agua, el cloruro de sodio sería el soluto y el agua sería el solvente.
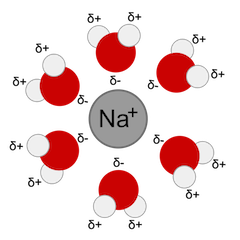 |
Una solución de electrolito es aquella en la que el soluto se disocia completamente o se rompe cuando se expone al solvente. Un ejemplo común es Gatorade, que los atletas consumen para reponer los electrolitos perdidos debido a la sudoración. Los principales electrolitos que contiene Gatorade son cloruro de sodio (sal de mesa), citrato de sodio y fosfato monopotásico.
Las soluciones de electrolitos se pueden analizar cuantitativamente en términos de su concentración, lo que significa cuánto soluto contienen por cantidad determinada de solvente. Veamos las unidades comunes de concentración y cómo calcularlas.
Molaridad
La molaridad es una medida de moles de soluto por litro de solución. Para calcular la molaridad, Rhonda solo necesita saber dos cosas: cuánto de nuestro soluto tiene (en moles) y cuánto solvente tiene (en litros).
Por ejemplo, suponga que Rhonda necesita conocer la molaridad de una solución que se obtiene disolviendo 0,505 moles de cloruro de sodio en 2 litros de agua. Simplemente dividiría 0.505 moles por 2 litros para obtener una concentración de 0.2525 M (moles por litro).
0,505 moles de NaCl / 2L = 0,2525 M
Molalidad
La molalidad es otra forma de expresar la concentración de la solución y es similar a nuestras unidades de molaridad anteriores. La molalidad es una medida de moles de soluto por kilogramo de disolvente.
Rhonda quiere calcular la molalidad de su solución que se obtiene al disolver 2.5 gramos de bromuro de potasio en 1000 kilogramos de agua. Simplemente tomaríamos 2.5 g divididos por 1000 kg y obtendríamos la molalidad de la solución en 0.0025 m, donde la letra minúscula ‘m’ siempre significa molalidad.
2,5 g / 1000 kg = 0,0025 m
Porcentaje por masa
El porcentaje en masa es la masa del soluto dividida por la masa de la solución x 100%. Entonces Rhonda necesita saber cuánto soluto tiene y también cuánta solución total tiene.
Siempre es importante darse cuenta de que la solución total se refiere a la cantidad de soluto MÁS la cantidad de disolvente. La mayoría de las veces, los problemas de porcentaje en masa se resuelven utilizando cantidades en gramos de soluto y disolvente. También es importante recordar que debido a que estamos hablando de un porcentaje, siempre debemos multiplicar por un factor de 100 para expresar nuestra respuesta como tal.
Si Rhonda necesita determinar cuál es el porcentaje en masa de cloruro de sodio en una solución compuesta por 3.45 gramos de cloruro de sodio en 45.0 gramos de agua, simplemente dividiría 3.45 gramos por 48.45 gramos (la masa total de la solución) y multiplicaría por 100 para obtener nuestra respuesta de 7,12%.
(3,45 g de NaCl / 48,45 g de masa total) x 100 = 7,12% de NaCL
Lo que esto le dice físicamente es que de la solución total, solo el 7.12% es cloruro de sodio y el resto es agua.
Resumen de la lección
Las soluciones de electrolitos están formadas por sustancias disueltas en agua para que la solución resultante conduzca la electricidad. En cualquier solución, siempre habrá un soluto (componente menor) y un solvente (componente principal). Algunas formas comunes de determinar las concentraciones de electrolitos dentro de la solución son:
- Molaridad : moles de soluto por litro de solución (mol / L). Tiene el símbolo ‘M’.
- Molalidad : moles de soluto por kilogramo de solución (mol / kg). Tiene el símbolo ‘m’.
- El porcentaje en masa se calcula tomando la masa del soluto y dividiéndola por la masa de la solución completa, luego multiplicando por 100.
Aprende más sobre:
Arte Arquitectura Biologia Ciencia Ciencia Fisica Ciencias de la Tierra Ciencias Sociales Economia Historia Historia Mundial Historia Moderna Medio Ambiente y Ecologia Literatura Plantas y Animales Religiones del Mundo QuimicaArticulos relacionados
- Uso de la ley de los gases ideales: calcular la presión, el volumen, la temperatura o la cantidad de un gas
- De lecciones de soluciones, electrolitos y no electrolitos
- Electrolito: definición y ejemplos
- Descripción general de los tipos de especiación y las barreras
- Ideas del proyecto STEM de platos de papel
- Química orgánica: Definición, importancia y ejemplos
- La teoría cinética molecular: propiedades de los gases
- Representación gráfica de la función tangente: amplitud, período, cambio de fase y desplazamiento vertical
- Metales pesados: definición y ejemplos
- AIBN: peso molecular, vida media y solubilidad
- Tipos de poliéster, estructura química y usos
- Ideas de proyectos de modelos de moléculas
- Fisión homolítica y heterolítica
- Descripción general del sistema solar
- Mezcla heterogénea: definición y ejemplos
