
Ecuación química equilibrada para la fotosíntesis
Introducción a la fotosíntesis
La mayoría de nosotros entendemos que necesitamos oxígeno para respirar y mantenernos vivos, y muchos saben que también exhalamos dióxido de carbono. Lo que quizás no sepa es cómo las plantas usan realmente el dióxido de carbono que exhalamos para producir azúcares para obtener energía y liberar el oxígeno que necesitamos para sobrevivir en el proceso.
Los seres humanos y los animales pasan por un proceso llamado respiración celular en el que se inhala oxígeno y se usa para ayudar a descomponer las moléculas de azúcar. En este proceso, se liberan dióxido de carbono, agua y energía.
La fotosíntesis es básicamente una imagen especular de la respiración celular en la que se utilizan agua, dióxido de carbono y energía del sol para generar azúcares, liberando oxígeno en el proceso.
Reacciones químicas
Una reacción química es el proceso en el que las sustancias se transforman en otras sustancias debido al reordenamiento de moléculas y átomos. Durante las reacciones químicas, no se crea ni se destruye nada, simplemente se cambia.
¡Las reacciones químicas ocurren a nuestro alrededor todos los días de nuestras vidas! La oxidación es una reacción química en la que el hierro, el agua y el oxígeno reaccionan para formar óxido de hierro (III) hidratado, que conocemos como óxido. Los mismos elementos están presentes al principio y al final de la reacción, simplemente han cambiado.
Los reactivos son las sustancias químicas que entran en la reacción y los productos son las sustancias químicas que salen de la reacción. En el ejemplo del óxido, el oxígeno, el agua y el hierro son los reactivos, mientras que el óxido de hierro (III) hidratado, u óxido, es el producto.
Las fórmulas químicas muestran la composición de una sustancia mediante el uso de números y letras. La fórmula química del agua se ve así:
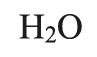 |
La H significa hidrógeno y la O significa oxígeno. El 2 después de la H indica que hay 2 átomos de hidrógeno por cada átomo de oxígeno. Los átomos son la partícula más pequeña de un elemento, mientras que las moléculas son dos o más átomos juntos. Por ejemplo, una molécula de agua está compuesta por tres átomos: dos átomos de hidrógeno y un átomo de oxígeno.
Al escribir reacciones químicas, las fórmulas químicas de las sustancias se utilizan para formar una ecuación química .
Reacciones químicas de la fotosíntesis
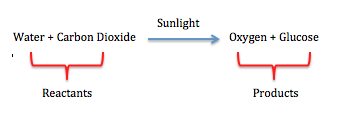
Analicemos la reacción química de la fotosíntesis.
- Los reactivos: dióxido de carbono y agua.
- Los productos: oxígeno y un azúcar llamado glucosa.
Aunque la luz solar es necesaria para la reacción, no se considera un reactivo porque solo se usa como fuente de energía. Las moléculas de la luz solar no se reorganizan ni se utilizan en los productos. Por esta razón, la luz solar se ve típicamente en la parte superior de la flecha en reacciones químicas.
 |
Para la ecuación, necesitaremos las fórmulas químicas para cada reactivo y producto.
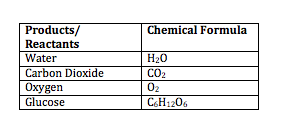 |
La ecuación química se escribe con los reactivos a la izquierda de la flecha y los productos a la derecha. La flecha indica que se ha producido una reacción y que los átomos y las moléculas se han reorganizado.
 |
Ecuación química equilibrada
Recuerde que nada se crea o destruye en una reacción química, por lo que los átomos en los reactivos deben ser iguales a los átomos en los productos. En otras palabras, la cantidad de átomos de carbono (C) a la izquierda de la flecha debe ser igual a los átomos de carbono a la derecha de la flecha. En nuestra reacción química hasta ahora, solo hay un átomo de C a la izquierda, mientras que hay seis átomos de C a la derecha.
Para equilibrar esta ecuación, también debe haber seis átomos de C a la izquierda. Podemos hacer esto agregando un gran ‘6’ delante de la molécula de dióxido de carbono. Al hacer esto, estamos diciendo que tiene que haber seis moléculas de dióxido de carbono en los reactivos.
También surge un problema similar con los átomos de hidrógeno (H); solo hay dos a la izquierda y doce a la derecha. Podemos lanzar otro ‘6’ delante de la molécula de agua para igualar los átomos (6 x 2 = 12).
¿Hemos terminado de equilibrar? ¡Todavía no! El problema ahora es que tenemos dieciocho átomos de oxígeno (O) a la izquierda y solo ocho a la derecha.
Para equilibrar los átomos de oxígeno, podemos agregar otro ‘6’ delante de la molécula de oxígeno de la derecha. Ahora finalmente tenemos una ecuación química balanceada con 12 átomos de hidrógeno, 18 de oxígeno y 6 de carbono a ambos lados de la flecha.
Resumen de la lección
La fotosíntesis es el proceso en el que las plantas utilizan la energía del sol para convertir el dióxido de carbono y el agua en glucosa y oxígeno. Esta ecuación química se muestra con las fórmulas químicas para cada uno de los reactivos y productos. Para equilibrar la ecuación, debemos asegurarnos de que los átomos de cada elemento sean iguales en el lado izquierdo y derecho de la reacción. Por ejemplo, el número de átomos de hidrógeno en los reactivos debe ser igual al número de átomos de hidrógeno en los productos.
Aprende más sobre:
Arte Arquitectura Biologia Ciencia Ciencia Fisica Ciencias de la Tierra Ciencias Sociales Economia Historia Historia Mundial Historia Moderna Medio Ambiente y Ecologia Literatura Plantas y Animales Religiones del Mundo QuimicaArticulos relacionados
- Fusión, fisión, datación por carbono, trazadores e imágenes: aplicaciones de la química nuclear
- Creación de argumentos y predicciones a partir de datos univariados
- Adivinando estrategias para los exámenes de materias SAT
- Cerio: descubrimiento de elementos y propiedades
- ¿Qué es el sulfato de potasio? – Estructura, usos y fórmula
- ¿Qué es el polietileno? – Propiedades y usos
- Oganesson: Usos y hechos de los elementos
- Tulio: Usos, Hechos y Propiedades
- Gráficos: tipos, ejemplos y funciones
- Lección de arsénico para niños: hechos y usos
- Gases perfectos: ley y ecuaciones
- ¿Qué es una aleación? – Definición y ejemplos
- Grupo de amina: estructura y ejemplos
- Uso de la recta numérica para comparar decimales, fracciones y números enteros
- Wilhelm Ostwald: Descubrimientos y contribución a la química
